一、热力学能的大小与哪些因素有关?是什么关系
与质量、体积、温度有关。
公式为:pV = nRT。
△U≡U终态-U始态,只要终态和始态一定,热力学的变化量△U是一定的。
没有外界影响的条件下,系统的各部分的宏观性质总会趋向一个长时期不发生变化的状态,称为平衡态。
当系统处于平衡态时,其状态参量才有确定的数值和意义。
处于平衡态的定量系统,其状态参量之间存在确定的函数关系,表示这种函数关系的数学关系称为该系统的状态方程。
扩展资料:达到热平衡的两物体的温度相等;
若把已经达到热平衡的两物体分开,则物体的状态将维持不变。
为了判别两个物体温度的高低,必须引进第三个物体,并依据基本实验事实。
若两个物体分别与处于确定状态的第三个达到热平衡,则这两个物体彼此也处于热平衡。
由于此实验事实是标定物体温度数值的基本依据。
参考资料来源:股票百科--热力学

二、热力学基础中,为什么热力学能的变化量等于热量Q加体积功W(恒压)啊?
热力学能的变化量等于热量Q加体积功W其中定义:能量增加为正 、吸热为正、 外界对气体做工为正。
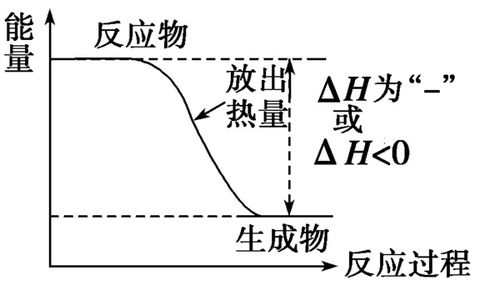
具体到吸热膨胀,气体对外做功,w=-pΔV为负值,热力学能的变化量等于“吸收”的热量“减去”系统因对外做体积功而损失的能量,即:ΔU=Q+w=Q-pΔV
三、热力学能的大小与哪些因素有关?是什么关系
与质量、体积、温度有关。
公式为:pV = nRT。
△U≡U终态-U始态,只要终态和始态一定,热力学的变化量△U是一定的。
没有外界影响的条件下,系统的各部分的宏观性质总会趋向一个长时期不发生变化的状态,称为平衡态。
当系统处于平衡态时,其状态参量才有确定的数值和意义。
处于平衡态的定量系统,其状态参量之间存在确定的函数关系,表示这种函数关系的数学关系称为该系统的状态方程。
扩展资料:达到热平衡的两物体的温度相等;
若把已经达到热平衡的两物体分开,则物体的状态将维持不变。
为了判别两个物体温度的高低,必须引进第三个物体,并依据基本实验事实。
若两个物体分别与处于确定状态的第三个达到热平衡,则这两个物体彼此也处于热平衡。
由于此实验事实是标定物体温度数值的基本依据。
参考资料来源:股票百科--热力学

四、热力学能U的改变量到底和过程有没有关系
1.热力学能改变量dE=吸热dQ-对外做功dA=300-200=100J 2.上升.气体的温度只与内能改变即热力学能改变有关,既然内能改变dE=100>0,所以温度上升

五、为什么热力学第二定律可以有许多不同的表述
1、克劳修斯表述: 不可能把热量从低温物体传向高温物体而不引起其它变化。
英国物理学家开尔文(原名汤姆逊)在研究卡诺和焦耳的工作时,发现了某种不和谐:按照能量守恒定律,热和功应该是等价的,可是按照卡诺的理论,热和功并不是完全相同的,因为功可以完全变成热而不需要任何条件,而热产生功却必须伴随有热向冷的耗散。
他在1849年的一篇论文中说:“热的理论需要进行认真改革,必须寻找新的实验事实。
”同时代的克劳修斯也认真研究了这些问题,他敏锐地看到不和谐存在于卡诺理论的内部。
他指出卡诺理论中关于热产生功必须伴随着热向冷的传递的结论是正确的,而热的量(即热质)不发生变化则是不对的。
克劳修斯在1850年发表的论文中提出,在热的理论中,除了能量守恒定律以外,还必须补充另外一条基本定律:“没有某种动力的消耗或其他变化,不可能使热从低温转移到高温。
”这条定律后来被称作热力学第二定律。
2、开尔文表述: 不可能制成一种循环动作的热机,从单一热源取热,使之完全变为功而不引起其它变化。
这是从能量消耗的角度说的。
开尔文表述还可以表述成:第二类永动机不可能实现。
开尔文的表述更直接指出了第二类永动机的不可能性。
敞处搬肺植镀邦僧鲍吉所谓第二类永动机,是指某些人提出的例如制造一种从海水吸取热量,利用这些热量做功的机器。
这种想法,并不违背能量守恒定律,因为它消耗海水的内能。
大海是如此广阔,整个海水的温度只要降低一点点,释放出的热量就是天文数字,对于人类来说,海水是取之不尽、用之不竭的能量源泉,因此这类设想中的机器被称为第二类永动机。
而从海水吸收热量做功,就是从单一热源吸取热量使之完全变成有用功并且不产生其他影响,开尔文的说法指出了这是不可能实现的,也就是第二类永动机是不可能实现的。

六、化工热力学问题
沿革 热力学是物理学的一个组成部分,它是在蒸汽机发展的推动下,于19世纪中叶开始形成的。
最初只涉及热能与机械能之间的转换,以后逐渐扩展到研究与热现象有关的各种状态变化和能量转换的规律。
在热力学的基本定律中,热力学第一定律表述能量守恒关系,热力学第二定律从能量转换的特点论证过程进行的方向。
这两个定律具有普遍性,在化学、生物学、机械工程、化学工程等领域得到了广泛的应用。
热力学基本定律应用于化学领域,形成了化学热力学,其主要内容有热化学、相平衡和化学平衡的理论;
热力学基本定律应用于热能动力装置,如蒸汽动力装置、内燃机、燃气轮机、冷冻机等,形成了工程热力学,其主要内容是研究工质的基本热力学性质以及各种装置的工作过程,探讨提高能量转换效率的途径。
化工热力学是以化学热力学和工程热力学为基础,在化学工业的发展中逐步形成的。
化工生产的发展,出现了蒸馏、吸收、萃取、结晶、蒸发、干燥等许多单元操作,以及各种不同类型的化学反应过程,生产的规模也愈来愈大,由此提出了一系列的研究课题。
例如在传质分离设备的设计中,要求提供多组分系统的温度、压力和各相组成间的相互关系的数学模型。
一般化学热力学很少涉及多组分系统,它不仅需要热力学,还需要应用一些统计力学和经验方法。
在能量的有效利用方面,化工生产所涉及的工作介质比工程热力学研究的工作介质(空气、蒸汽、燃料气等)要复杂得多,且能量的消耗常在生产费用中占有很高比例,因此更需要研究能量的合理利用和低温位能量的利用,并建立适合于化工过程的热力学分析方法。
1939年,美国麻省理工学院教授H.C.韦伯写出了《化学工程师用热力学》一书。
1944年,美国耶鲁大学教授 B.F.道奇写出了名为《化工热力学》的教科书。
这样,化工热力学就逐步形成为一门学科。
随着化学工业规模的扩大,新过程的开发,以及大型电子计算机的应用,化工热力学的研究有了较大的发展。
世界各国化工热力学专家在1977年举行了首届流体性质和相平衡的国际会议,1980和1983年分别举行了第二届和第三届会议,还出版了期刊《流体相平衡》。
化工热力学已列为大学化学工程专业的必修课程。

七、什么时候焓变与热力学能相差最大
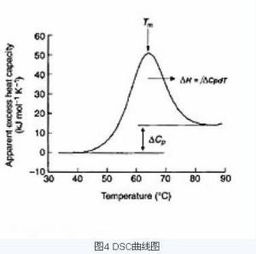
(焓变)即物体焓的变化量。
焓是物体的一个热力学能状态函数,即热函:一个系统中的热力作用,等于该系统内能加上其体积与外界作用于该系统的压力的乘积的总和。
也就是说系统对外做功越大其焓变与内能相差越大。
参考文档
声明:本文来自网络,不代表【股识吧】立场,转载请注明出处:https://www.gupiaozhishiba.com/store/62080576.html



 大目老师
大目老师
发表于 2023-07-27 22:04回复 尔晴结局:大气温度随着高度变化的理论依据是热力学理论。首先,大气温度的垂直分布受到太阳辐射、地球表面温度和大气组成等多种因素的影响。在近地面层,大气温度受到地表辐射吸收和长波辐射的影响,因此温度随高度变化较小,通常在1km内... [详细]