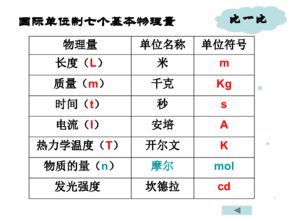
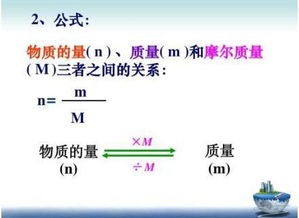
一、物质的量与质量之比
1、质量=物质的两*摩尔质量一般来说,各常见元素的摩尔质量都不同,所以物质的量与质量的比一般不一样,相差一个摩尔质量之比。
eg:Fe的摩尔质量=56;
Zn的摩尔质量=65,所以:1mol的Zn与1mol的Fe的质量比=1*65/(1*56)=65/56。
其余的原子分子或者单质化合物之间等等,都是这么换算。
2、当两个物质的摩尔质量相同的时候物质的量与质量比值相同,eg:1mol的Ca与1mol的NaOH的质量比就是1*40/(1*40)=1当然,采用的不是精确的摩尔质量值计算的。
二、怎样确定化学反应中各物质的质量比
反应物的质量减少,而生成物的质量会增加甲:由20 变为0,减少20 ,乙:由5变为5,没变。
丙:由80变为10,减少70。
丁:由30变为120,增加90。
所以,乙可能是反应的催化剂,也可能与反应无关。
甲、丙、丁三种物质的质量比为:2:7:9
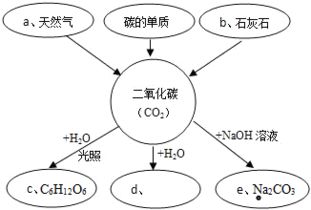
三、如何计算化学元素中的质量分数与质量比?

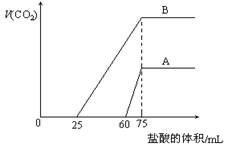
四、两种物质怎么求它们的物质的量之比
33.6/22"利用公式物质的量=物质的质量/物质的摩尔质量(摩尔质量在数值上等于查对分子质量)若的气体的则物质的量=气体的体积/气体的摩尔体积(气体的摩尔体积=22.4L)如16gO2与14gN2的物质的量之比16/28=1:111.2LO2与33.6LN2的物质的量之比11.2/22.4.4=1;
32:14/
五、怎么求物质的质量比
元素的质量比=(相对原子质量*原子个数)之比如:水H2O中氢、氧元素的质量比m(H):m(O)=1*2:16=1:8再如:氯酸钾KClO3中三种元素的质量比=39:35.5:16*3=39:35.5:48又如:某氮的氧化物中氮、氧元素的质量比为7:4,求该氧化物的化学式。
解:设氧化物的化学式为NxOy,则由化学式可得氮、氧质量比为14X:16Y与题目所给联立得:14X:16Y=7:4解出:X:Y=2:1所以,化学式为N2O
六、由质量比如何求物质的量比
把公式m=nM代入比值等式化简即得

七、怎样求得物质的分子质量比?
1比32比18就是将它们的每个原子的原子质量相加比如水:H2O 其中有两个H 和一个OH的原子质量是1 而O的原子质量是16所以H2O=1*2+16=18懂吗.其他也一样算的

八、化学方程式中各物质之间质量比怎么求
各物质质量之比等于系数乘以式量之比

参考文档
声明:本文来自网络,不代表【股识吧】立场,转载请注明出处:https://www.gupiaozhishiba.com/read/33493573.html



