一、研究卫星绕地球运行周期时可以把地球和卫星都看作质点 为什么
卫星——体积很小,相对于轨道半径来说可以忽略。
地球——并不是因为地球半径可忽略,而是因为,地球是球体,它的大小和形状对所研究的问题没有影响,完全可以用质点来代替。
例如,计算比较近的球体的万有引力,也可以把球体看做质点。

二、离子化合物比较熔沸点中电荷数和离子半径怎么看?
电荷:2+1可以这样判断只考虑一个即可Cl-到Mg2+之间的距离

三、分子晶体为什么较脆
①根据导电性判断 熔化或固态时都不导电的一般是原子晶体或分子晶体;
熔化或固态都能导电的一般为金属晶体;
固态时不导电,熔化或溶于水时能导电的一般为离子晶体;
熔化、固态都不能导电,但溶于水后大多导电的晶体一般是分子晶体。
石墨称为过渡型或混合型晶体能导电。
②根据机械性能判断 具有高硬度的为原子晶体,较硬且脆的为离子晶体,硬度较差但较脆的为分子晶体,有延展性的为金属晶体。
③根据熔、沸点判断 离子晶体与原子晶体熔、沸点高于分子晶体。
金属晶体熔沸点有的高,有的低。
四种基本晶体熔、沸点对比规律1、一般: 原子晶体>离子晶体>金属晶体>分子晶体2、各自比较: ①离子晶体:离子半径小(或阴、阳离子半径之和越小的),离子所带电荷数越多,键能越强,熔、沸点就越高。
②分子晶体:在组成结构均相似的分子晶体中,式量大的分子间作用力就大,熔沸点高;
分子极性大,熔沸点高;
但分子间有氢键存在的物质熔沸点偏高。
③原子晶体:成键原子半径小,键能大,熔沸点就高。
④金属晶体:金属离子半径越小,电荷数越多,其熔沸点越高。

四、铜和锌的质子数比铁钴镍多,为什么原子半径反而更大
球层的总电荷量为Q=[4Пρ(R2^3-R1^3)]/3所求电势为:V=Q/(K*r) (其中K=9.0*10^9 为系数)因球层为均匀,故可用公式V=Q/(K*r)

五、为什么当直角三角形斜边一定时,当它是等边直角三角形时面积最大?
几何法:直角三角形面积S=a×b/2,其中a为斜边,b为斜边上的高。
如果a确定,则只需要b为最大值时,三角形面积就是最大值。
直角三角形当斜边一定时就可以确定唯一一个外接圆,这个圆是以斜边长a为直径。
直角所在的点在圆上移动时,当这一点与圆心的连线垂直时,连线即为斜边的高,同时也是最大的b值,此时b=a/2,而这正是一个等边直角三角形。
代数法:S=c*d/2 c、d为两直角边c=(a^2-d^2)^(1/2) a为斜边S=d*(a^2-d^2)^(1/2)/2S^2=d^2*(a^2-d^2)/4≤(d^2+(a^2-d^2))^2/16=a^2/4当:d^2=(a^2-d^2)时取最大值,即d=a×2^(1/2)/2这是一个等边直角三角形不知道能不能看明白
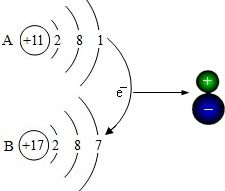
六、铜和锌的质子数比铁钴镍多,为什么原子半径反而更大
因为铜锌的3d亚层全满。
所以半径更大
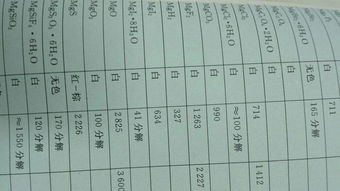
七、MgO,GaO,SrO,BaO的熔点和硬度依次降低吗?为何?
Mg,Ca,Sr,Ba同为第二主族,原子半径依次增大,离子半径也是依次增大(多一层电子嘛),它们对应的氧化物为离子晶体,离子晶体的熔点和硬度主要取决于离子间静电作用力,而静电力F=k*Q1*Q2/R^2,显然MgO,GaO,SrO,BaO晶体的静电力依次减弱(因为离子晶体离子间靠得还是很近的,离子半径对R有很大影响),所以MgO,GaO,SrO,BaO的熔点和硬度依次降低
八、关于电荷体密度的难题
球层的总电荷量为Q=[4Пρ(R2^3-R1^3)]/3所求电势为:V=Q/(K*r) (其中K=9.0*10^9 为系数)因球层为均匀,故可用公式V=Q/(K*r)

参考文档
下载:为什么衰变半径只比较电荷量.pdf《拿一只股票拿多久》《德新交运股票停牌多久复牌》《新的股票账户多久可以交易》《股票赎回到银行卡多久》《场内股票赎回需要多久》下载:为什么衰变半径只比较电荷量.doc更多关于《为什么衰变半径只比较电荷量》的文档...声明:本文来自网络,不代表【股识吧】立场,转载请注明出处:https://www.gupiaozhishiba.com/author/61800288.html



