一、S轨道和P轨道什么意思..?请尽量说清楚一点.语言别太专业
其实,这只是一个代号而已。
每个原子,外层电子都有个排列规则,比如最内层两个电子,次内层和最外层八个电子等等之类的排列规则。
那么每个电子层之间,我们可以把它当作每个相对独立的空间。
每个空间之内的电子,因为拥有不同的能量,所处的空间位置也不一样。
这个空间位置的不一样,不是想象出来的,好像是根据薛定谔方程可以算出来(具体的你就别算了,要算你这一辈子也别干别的了),也就是我们常说的轨道。
轨道的划分,不是用原因可以解释的,所以如果要记住,就只能背了。
好在不难,轨道的标记分别为s、p、d、e、f、g........,除了之前的两个,后面是按照字母排列的。
每个轨道对应的轨道数分别是1、3、5、7.......。
先给你解释到这儿,不明白可以追问或者加QQ345017627
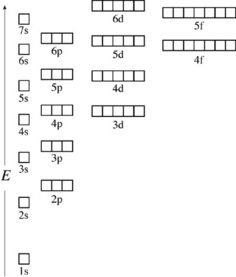
二、加入磁场s.p能级分裂,为什么原子中p能级比s能级高
A、H、He原子核外p能级、d能级等原子轨道上电子排布为“全空”,H原子核外只有一个电子,未达到稳定结构,He原子核外有2个电子,已经达到稳定结构,所以不能用此来判断第一电离能的大小,故A错误;
B、26Fe2+容易失电子转变成26Fe3+,失去电子时都是从外到内失去,铁离子也容易得电子生成亚铁离子,所以不能用此规律来判断,故B错误;
C、基态铜(Cu)原子的电子排布式为[Ar]3d104s1而不是[Ar]3d94s2,[Ar]3d104s1中d轨道处于全满,s轨道处于半满,所以能用此规律来判断,故C正确;
D、激发态的原子是基态原子吸收能量后发生电子跃迁形成的,所以不能用此规律来判断,故D错误;
故选C.

三、S轨道和P轨道什么意思..?请尽量说清楚一点.语言别太专业
其实,这只是一个代号而已。
每个原子,外层电子都有个排列规则,比如最内层两个电子,次内层和最外层八个电子等等之类的排列规则。
那么每个电子层之间,我们可以把它当作每个相对独立的空间。
每个空间之内的电子,因为拥有不同的能量,所处的空间位置也不一样。
这个空间位置的不一样,不是想象出来的,好像是根据薛定谔方程可以算出来(具体的你就别算了,要算你这一辈子也别干别的了),也就是我们常说的轨道。
轨道的划分,不是用原因可以解释的,所以如果要记住,就只能背了。
好在不难,轨道的标记分别为s、p、d、e、f、g........,除了之前的两个,后面是按照字母排列的。
每个轨道对应的轨道数分别是1、3、5、7.......。
先给你解释到这儿,不明白可以追问或者加QQ345017627

四、量子力学中,为什么s才一个轨道?p有三轨道?d有5轨道
1、这是客观存在的规律,被人们发现2、你只需要记忆,并会应用3、电子云的伸展方向决定

五、纳原子3s、3p、3d轨道的能量高低我,以及为什么
展开全部3s<3p<3d,简单点可认为离核远近不同

六、为什么s轨道,p轨道重叠。有方向性。s轨道与s轨道。没有方向性。
s轨道的电子运为球形对称,任何方向的电子云密度都相等,任何方向成键想过都一样,故没有方向性。
p轨道不同的方向,电子运的密度不同,只有电子用密度大的方向可以成键,所以有方向性。
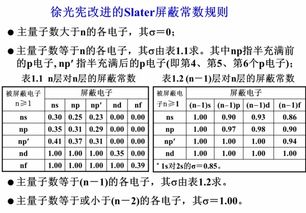
七、量子力学中,为什么s才一个轨道?p有三轨道?d有5轨道
1、这是客观存在的规律,被人们发现2、你只需要记忆,并会应用3、电子云的伸展方向决定

参考文档
下载:为什么p轨道比s轨道能量大.pdf《东方财富股票质押多久》《股票你们多久看一次》《股票买入委托通知要多久》《川恒转债多久变成股票》下载:为什么p轨道比s轨道能量大.doc更多关于《为什么p轨道比s轨道能量大》的文档...声明:本文来自网络,不代表【股识吧】立场,转载请注明出处:https://www.gupiaozhishiba.com/article/18733172.html



 郑雄仁
郑雄仁
发表于 2023-08-10 13:06回复 逸品馆:轨道能量高低顺序是:p轨道>sp3杂化轨道>sp2杂化轨道>sp杂化轨道>s轨道。sp3d2杂化轨道如下图所示:... [详细]