一、定熵过程的系数为什么是等压比热容与等容比热容比值
dG=-SdT+Vdp+μdNT----温度、G----吉布斯自由能、V----体积、μ----化学势、N----物质粒子数、p----压强、S-----熵等温等压→dT=0、dp=0 则dG=μdN,也就是最大的非体积功,这便是可逆的情况。

二、为什么物体的定压比热容比定体比热容大
定压的加热的时候不光使物体温度升高还赋予了物体做外做功的能力。
有压力物体就有流动趋势。
定压比定容多了一个物体间的推动功。

三、共轭更稳定,书上写着CC单键较为稳固,故跃迁需要较高的能量,为什么共轭双键跃迁所需的能量降低?
首先你要知道紫外光谱的测量范围是在200nm-400nm左右,共轭双键由于形成了以C=C-C=C的π-π共轭效应,形成的大π健较稳定,吸收范围大概在217~280nm。
因此当被检测物质含有共轭双键时,在以波长为横坐标,吸收度A为纵坐标的紫外光谱上你就会看到在200nm左右会出现吸收峰,这就表明了紫外光谱的原理。
其实光谱学起来挺有趣的!!!我也很喜欢。
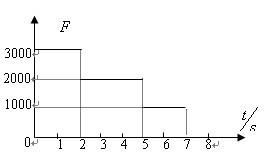
四、质量为2.8g,温度为300K,压强为1atm的N2,等压膨胀到原体积的两倍
氮气视为理想气体 N2的量n=2.8/28=0.1mol,压强P1=P2=1atm=101325Pa, 始态体积V1=nRT1/P=0.1*8.314*300/101325=2.46*10^-3(m3) ,T1=300K 终态体积V2=2V1=4.92*10^-3m3,T2=P2V2/(nR)=101325*4.92*10^-3/(0.1*8.314)=600K 等压膨胀,压强不变,则氮气所作的功W=-P*ΔV=-101325*(4.92*10^-3-2.46*10^-3)=-249.4(J) 理想气体的内能只与温度有关,双原子刚性气体分子的摩尔等容热容Cv,m=2.5R 所以内能变化ΔU=nCv,mΔT=0.1*2.5*8.314*(600-300)=623.6(J) 根据热力学第一定律Q=ΔU-W=623.6-(-249.4)=873(J)
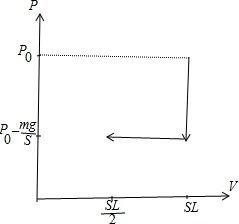
五、相同条件的理想气体的恒温可逆压缩和绝热可逆压缩相同体积为什么终态不同,恒温的压强要大?
绝热过程:p1的V ^γ= p2的(V / 2)^γ, P1 V = NRT1,P2 V / 2 = NRT2 T2:T1 = p2的:2P1 = 2 ^(γ-1) 单原子γ= CP / CV = 5/3 因此,T2:T1 = 2 ^(2/3) Tαv^ 2 v2的:第一版= 2 ^(1/3)
六、一定量的理想气体等压膨胀温度怎么变化,此时吸热量与对外做工消耗量谁大谁小?
展开全部一定量的理想气体等压膨胀,会吸热,吸热应该比对外做工小

七、热容 定体热容 定压热容和内能 熵 热量的关系
定压热容与定体热容的比值称为摩尔热容比,用符号γ表示,大小等于(i+2)/i,其中i是理想气体的自由度。
摩尔定压热容: 气体的摩尔定压热容,是指1mol气体在压强不变而且没有化学反应与相关的条件下,温度改变1K(或1度)所吸收或放出的热量,用Cp表示,其数值可以由实验测定。
气体的摩尔定体热容,是指1mol气体在体积不变而且没有化学反应与相关的条件下,温度改变1K(或1度)所吸收或放出的热量,用Cv表示,其数值可以由实验测定。

参考文档
下载:为什么等压比等体需要的热量大.pdf《已经卖出的股票的钱什么时候能取出》《海什么医药股票查询》《借壳上市为什么要增加股本》《股票代码前面带上xd是什么意思》《五行缺火八字喜金可以炒股吗》下载:为什么等压比等体需要的热量大.doc更多关于《为什么等压比等体需要的热量大》的文档...声明:本文来自网络,不代表【股识吧】立场,转载请注明出处:https://www.gupiaozhishiba.com/article/17923358.html


 花木呈祥
花木呈祥
发表于 2023-07-22 04:49回复 宋玉淑:会飞,可是不善于飞行。蟑螂体扁平,黑褐色,通常中等大小。头小,能活动。触角长丝状,复眼发达。翅平,前翅为革质后翅为膜质,前后翅基本等大,覆盖于腹部背面;有的种类无翅。不善飞,能疾走。不完全变态。产卵于卵鞘... [详细]